|
Votre recherche : Ensemble de gaine d'introduction Edwards eSheath+
Dossier d'information Euro-Pharmat
Dispositif médical

|
Dossier d'information Euro-Pharmat
Dispositif médical
|
| Ensemble de gaine d'introduction Edwards eSheath+ |
| |
|
|
Date de mise à jour : |
30/11/2023 12:09:59
|
| 1. Renseignements administratifs concernant l'entreprise |
| 1.1 |
Nom : |
EDWARDS LIFESCIENCES SAS |
| 1.2 |
Adresse : |
1 rue Arnold Schoenberg
78280 GUYANCOURT
|
| Tél. : |
|
| Fax : |
|
| e-mail : |
sara_delannay@edwards.com
|
| Site : |
http://www.edwards.com
|
| 1.3 |
Correspondant matériovigilance : |
Maite LLACER |
| Tél. : |
+34 96 305 37 14 |
| Fax : |
+33 1 30 05 29 64 |
| e-mail : |
complaints_INTL_TMTT@edwards.com
|
| 4. Conditions de conservation |
| |
Conditions normales de conservation et de stockage : |
| Doit être conservé dans un endroit frais et sec. |
| Précautions particulières : |
| L’outil d’extension n’est pas recouvert d’un matériau hydrophile. Ne pas l’utiliser comme dilatateur.
La gaine s’élargit provisoirement pour permettre le passage de dispositifs ; s’assurer que la structure vasculaire peut accueillir le diamètre maximal de la gaine.
Toujours maintenir l’orientation de la position de la gaine lors de l’insertion, de la manipulation ou du retrait d’un dispositif par la gaine.
En cas de ponction, de suture ou d’incision du tissu à proximité de la gaine, prendre les précautions nécessaires pour éviter d’endommager la gaine.
Il convient de faire preuve de prudence dans les vaisseaux dont le diamètre est inférieur à 5,5 mm ou 6mm, car cela peut empêcher la mise en place sure de l’ensemble de gaine d’introduction Edwards eSheath+ 14F et 16F, respectivement.
Faire preuve de prudence dans des vaisseaux tortueux ou calcifiés qui pourraient empêcher l’introduction de sûre de gaine d’introduction.
|
| Durée de validité du produit : |
| |
| Présence d'indicateurs de température (s'il y a lieu) : |
| |
| 5. Sécurité d'utilisation |
| 5.1 |
Sécurité technique : |
| |
| 5.2 |
Sécurité biologique (s'il y a lieu) : |
| |
| 6. Conseils d'utilisation |
| 6.1 |
Mode d'emploi : |
| |
| 6.2 |
Indications (destination marquage CE) : |
| Indiqué pour l'introduction et le retrait des systèmes de valve cardiaque transcathéter SAPIEN 3 et SAPIEN 3 Ultra dans le système vasculaire. |
| 6.3 |
Précautions d'emploi : |
| |
| 6.4 |
Contre indications (absolues et relatives) : |
| |
| 7. Informations complémentaires sur le produit |
| |
Informations complémentaires : |
| |
| 8. Documents annexés au dossier DM |
| |
|
| 9. Images (photos, étiquettes...) |
| |
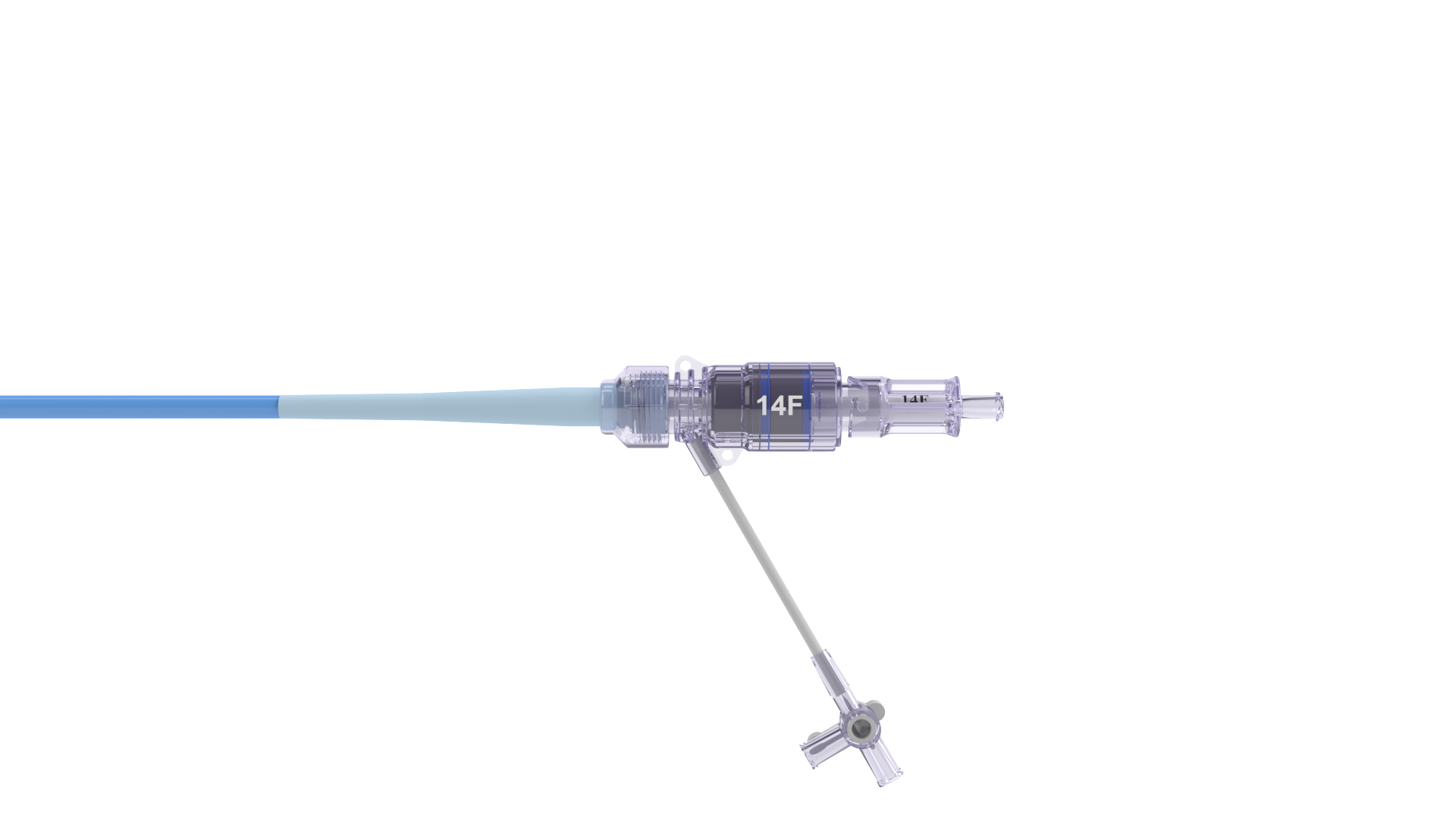


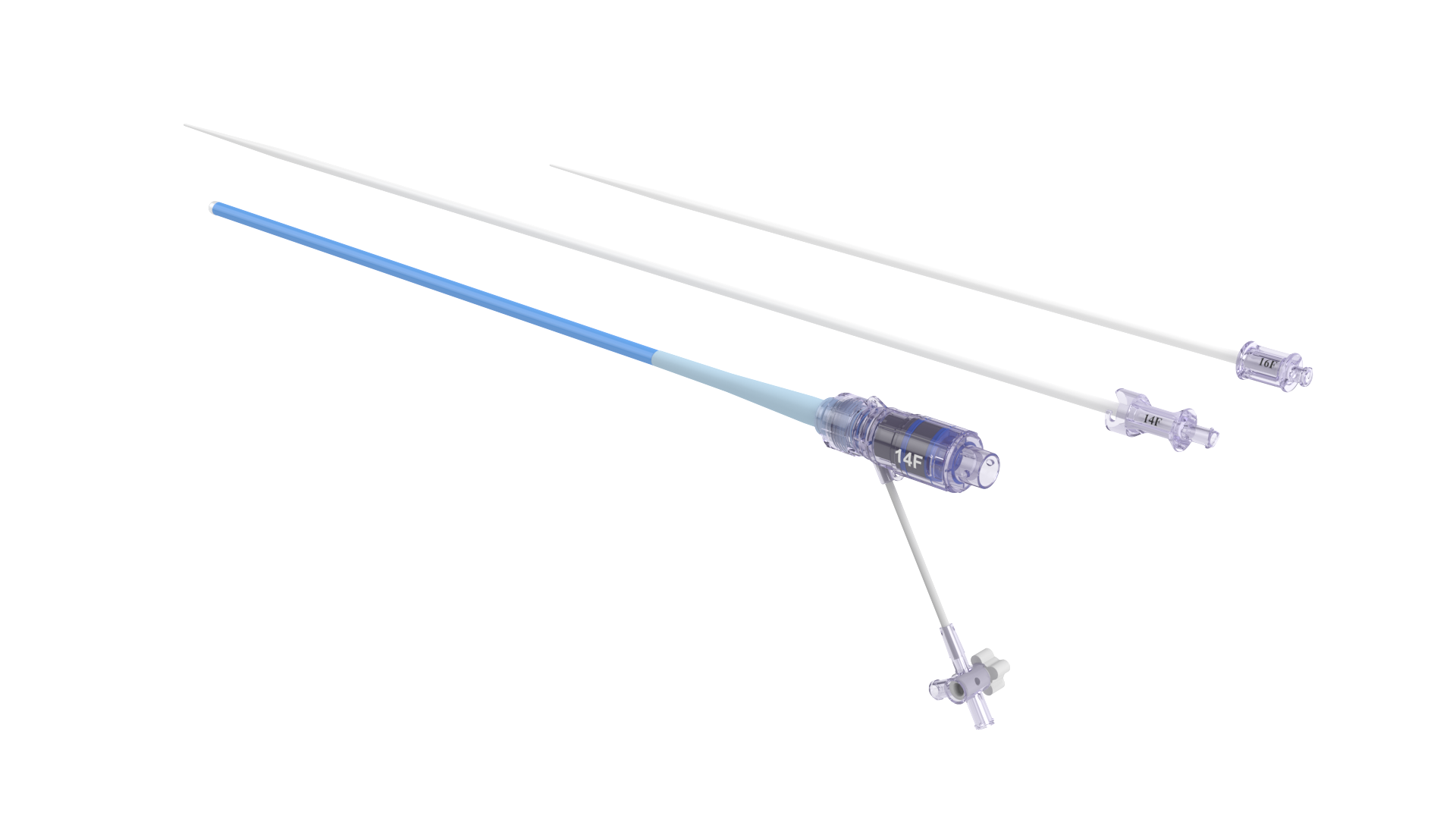
|
Télécharger PDF Creator pour imprimer au format PDF
|