|
Votre recherche : Penumbra System RED72 SENDit Kit
Dossier d'information Euro-Pharmat
Dispositif médical

|
Dossier d'information Euro-Pharmat
Dispositif médical
|
| Penumbra System RED72 SENDit Kit |
| |
|
|
Date de mise à jour : |
02/07/2024 18:18:02
|
| 1. Renseignements administratifs concernant l'entreprise |
| 1.1 |
Nom : |
PENUMBRA FRANCE SAS |
| 1.2 |
Adresse : |
3 bd de Sébastopol
75001 Paris
|
| Tél. : |
0805101183 |
| Fax : |
0805101189 |
| e-mail : |
de-info@penumbrainc.com
|
| Site : |
https://www.penumbrainc.com/
|
| 1.3 |
Correspondant matériovigilance : |
Jens Pfannkuche |
| Tél. : |
+49302005676219 |
| Fax : |
+493069088045 |
| e-mail : |
jpfannkuche@penumbrainc.com
|
| 2. Informations sur dispositif ou équipement |
| 2.1 |
Dénomination commune selon la nomenclature Euro-Pharmat : |
SET THROMBOASPIRATION CEREBRAL |
| 2.2 |
Dénomination commerciale : |
Penumbra System RED72 SENDit Kit |
| 2.3 |
Code Nomenclature : |
58173 (Cathéter), 16779 (Tubulure d'aspiration) |
| Code CLADIMED : |
C51BA |
| 2.4 |
Code LPPR* (Ex TIPS) si applicable :
* Liste des produits et prestations remboursables inscrits sur la liste prévue à l'article L165-1
|
N/A |
| 2.5 |
Classe du DM : |
III, IIa |
| Directive de l'UE applicable : |
Règlement européen 2017/745 relatif aux dispositifs médicaux |
| N° Organisme notifié : |
2797 |
| Première mise sur le marché dans l'UE : |
21/03/2024 |
| Fabricant : |
Penumbra Inc. |
| 2.6 |
Descriptif du dispositif : |
|
| Le Penumbra System® est composé de plusieurs dispositifs :
• Cathéter de reperfusion Penumbra
• Pompe d’aspiration Penumbra
• Réservoir de la pompe d’aspiration Penumbra
• Tubulure d’aspiration Penumbra
Le cathéter de reperfusion permet de cibler l’aspiration de la pompe directement sur le thrombus. Le cathéter de reperfusion est introduit par un cathéter guide ou une longue gaine dans le système vasculaire intracrânien et acheminé sur un fil guide neurovasculaire jusqu’au site de l’occlusion primaire.
La technologie SENDit peut être utilisée avec son cathéter de reperfusion préemballé pour faciliter l’accès à l’occlusion primaire. Le cathéter de reperfusion Penumbra est utilisé conjointement avec la pompe d’aspiration pour aspirer le thrombus et l’extraire du vaisseau occlus. Pour la source d’aspiration, le cathéter de reperfusion
Penumbra est utilisé conjointement avec la pompe d’aspiration Penumbra, qui est connectée à l’aide du réservoir de pompe d’aspiration Penumbra et de la tubulure d’aspiration Penumbra.
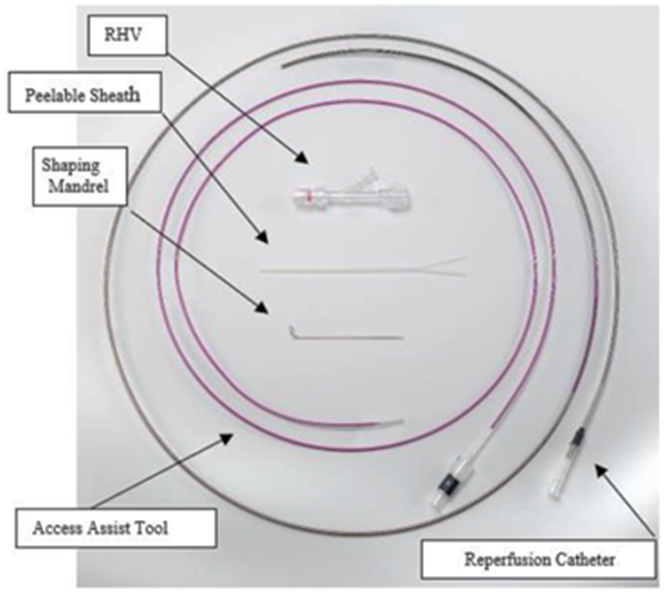
Le cathéter de reperfusion Penumbra est fourni avec un mandrin de modelage à la vapeur, une valve hémostatique rotative, une gaine pelable et, en option, la technologie SENDit. La compatibilité de la technologie SENDit se limite à son cathéter de reperfusion préemballé. Les dispositifs sont visibles sous radioscopie. Les cathéters de reperfusion du Penumbra System comportent un revêtement hydrophile sur le segment distal de la tige du cathéter (voir tableau 1).
La technologie SENDit est pré-assemblée à l'intérieur du Cathéter de Reperfusion RED 72 de manière à s'étendre de 1,5 cm (réf) au-delà du RED 72 associé. Lors de son utilisation, le Cathéter de Reperfusion RED 72 avec la technologie SENDit est guidé sur un guide standard jusqu'au site de l'occlusion en utilisant des techniques conventionnelles de guide. La technologie SENDit est utilisée uniquement pendant la livraison du RED 72 au site de l'occlusion. Une fois que le Cathéter de Reperfusion RED 72 avec la technologie SENDit est guidé jusqu'au site cible, la technologie SENDit est retirée avant l'utilisation du Cathéter de Reperfusion RED 72 pour l'aspiration. |
| 2.7 |
Références catalogue : |
|
Référence :
RED72SDKIT
Descriptif :
Cathéter de reperfusion RED 72 avec la technologie SENDit et tubulure d’aspiration
Conditionnement :
UCD Unité de commande : 1 BLISTER(S) PELABLE(S)
CDT Conditionnement : 1 BOITE(S)
QML Quantité mimimale de livraison : 1 UNITE(S)
Caractéristique(s) :
| |
|
| 2.8 |
Composition du dispositif et accessoires : |
| Principaux composants et matériaux :
|
|
Non renseigné
|
| Substances actives : |
|
|
|
Pour les composants suceptibles d'entrer en contact avec le patient et/ou les produits administrés, précisions complémentaires
|
| Latex : |
Non |
| Phtalates : |
Non |
| Origine animale ou biologique : |
Non |
| Dispositifs et accessoires associés (consommables captifs notamment) : |
| |
| 2.9 |
Domaines et indications (selon nomenclature Euro-Pharmat) : |
| Domaines : |
|
|
| Indications (Informations complémentaires au paragraphe 6) : |
|
|
| 4. Conditions de conservation |
| |
Conditions normales de conservation et de stockage : |
| • Conserver dans un lieu frais et sec.
• Éliminer le dispositif conformément à la politique de l’hôpital, de l’administration et/ou du gouvernement local. |
| Précautions particulières : |
| • Le Penumbra System doit être utilisé uniquement par des médecins ayant reçu la formation adéquate aux techniques interventionnelles neuro-endovasculaires et au traitement d’un accident vasculaire cérébral ischémique aigu.
• Utiliser avant la date de péremption.
• Utiliser le Penumbra System sous contrôle radioscopique.
• Comme dans toutes les interventions sous radioscopie, envisager de prendre toutes les précautions nécessaires pour limiter l’exposition du patient aux rayonnements en utilisant un écran de protection adéquat, des temps de radioscopie réduits, et en modifiant les facteurs techniques liés aux rayonnements lorsque cela est possible.
• Maintenir une perfusion constante de soluté de rinçage approprié.
• Lors de l’aspiration, s’assurer que la tubulure d’aspiration Penumbra n’est ouverte que pendant la durée minimale nécessaire à l’extraction du thrombus. Il est déconseillé d’effectuer une aspiration excessive ou de ne pas fermer la tubulure d’aspiration Penumbra quand l’aspiration est terminée.
• Comme pour toutes les interventions chirurgicales, il est recommandé de surveiller les pertes de sang intra-procédurales afin d’assurer une prise en charge appropriée.
• Éviter d’utiliser de l’alcool, des solutions antiseptiques ou d’autres solvants pour le traitement préalable du dispositif afin d’éviter des modifications imprévisibles du revêtement qui pourraient affecter la sécurité et les performances du dispositif. |
| Durée de validité du produit : |
| |
| Présence d'indicateurs de température (s'il y a lieu) : |
| |
| 5. Sécurité d'utilisation |
| 5.1 |
Sécurité technique : |
| |
| 5.2 |
Sécurité biologique (s'il y a lieu) : |
| |
| 6. Conseils d'utilisation |
| 6.1 |
Mode d'emploi : |
| |
| 6.2 |
Indications (destination marquage CE) : |
| Le Penumbra System est conçu pour extraire le thrombus et rétablir le flux sanguin dans le système neurovasculaire par aspiration. |
| 6.3 |
Précautions d'emploi : |
| |
| 6.4 |
Contre indications (absolues et relatives) : |
| |
| 7. Informations complémentaires sur le produit |
| |
Informations complémentaires : |
| |
| 8. Documents annexés au dossier DM |
| |
|
| 9. Images (photos, étiquettes...) |
| |

la6Hc-gsx0uSfSfMhGsgwg.png)
lZILU6k7906qebSCEnj0OQ.png)
TgICqg1U3Ei3FWgGl1DsAg.png)

SuTAj5xt70qe17BcFlOqDA.png)


|
Télécharger PDF Creator pour imprimer au format PDF
|