|
Votre recherche : SYSTEME DE DRAINAGE ASEPT
Dossier d'information Euro-Pharmat
Dispositif médical

|
Dossier d'information Euro-Pharmat
Dispositif médical
|
| SYSTEME DE DRAINAGE ASEPT |
| |
|
|
Date de mise à jour : |
11/12/2025 10:16:21
|
| 1. Renseignements administratifs concernant l'entreprise |
| 1.1 |
Nom : |
PFM MEDICAL FRANCE |
| 1.2 |
Adresse : |
6 rue Joule
Tourmaline 2
33700 MERIGNAC
|
| Tél. : |
05 56 02 77 35 |
| Fax : |
05 56 02 97 93 |
| e-mail : |
cscfrance@pfmmedical.com
|
| Site : |
http://www.pfmmedical.com
|
| 1.3 |
Correspondant matériovigilance : |
BERRIER CHRISTINE |
| Tél. : |
05 56 02 77 35 |
| Fax : |
05 56 02 97 93 |
| e-mail : |
cscfrance@pfmmedical.com
|
| 2. Informations sur dispositif ou équipement |
| 2.1 |
Dénomination commune selon la nomenclature Euro-Pharmat : |
DRAIN THORACIQUE |
| 2.2 |
Dénomination commerciale : |
SYSTEME DE DRAINAGE ASEPT |
| 2.3 |
Code Nomenclature : |
47797 |
| Code CLADIMED : |
|
| 2.4 |
Code LPPR* (Ex TIPS) si applicable :
* Liste des produits et prestations remboursables inscrits sur la liste prévue à l'article L165-1
|
|
| 2.5 |
Classe du DM : |
IIb |
| Directive de l'UE applicable : |
93/42/EEC |
| N° Organisme notifié : |
DEKRA CE0124 |
| Première mise sur le marché dans l'UE : |
01/01/2013 |
| Fabricant : |
pfm medical mepro gmbh |
| 2.6 |
Descriptif du dispositif : |
|
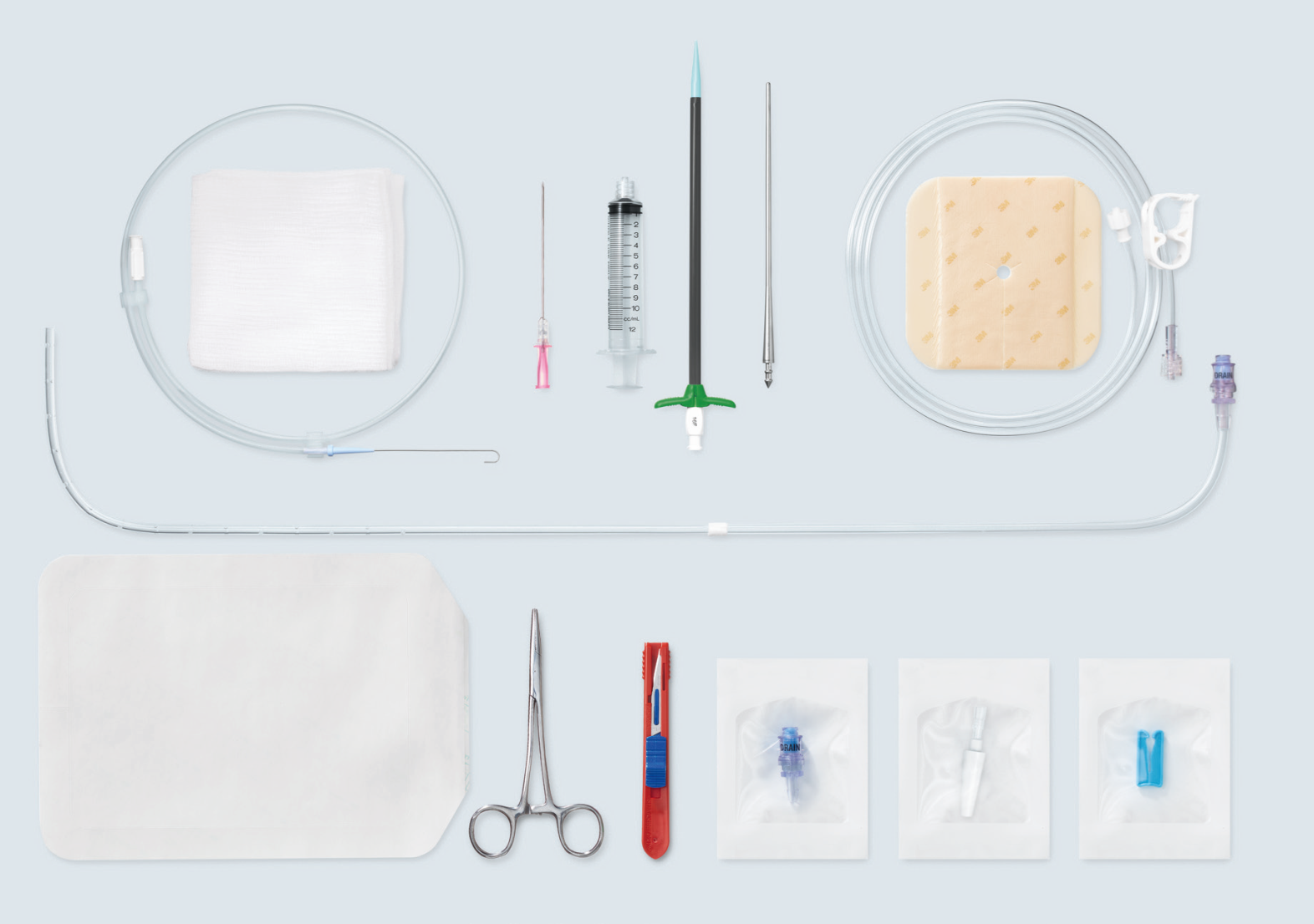
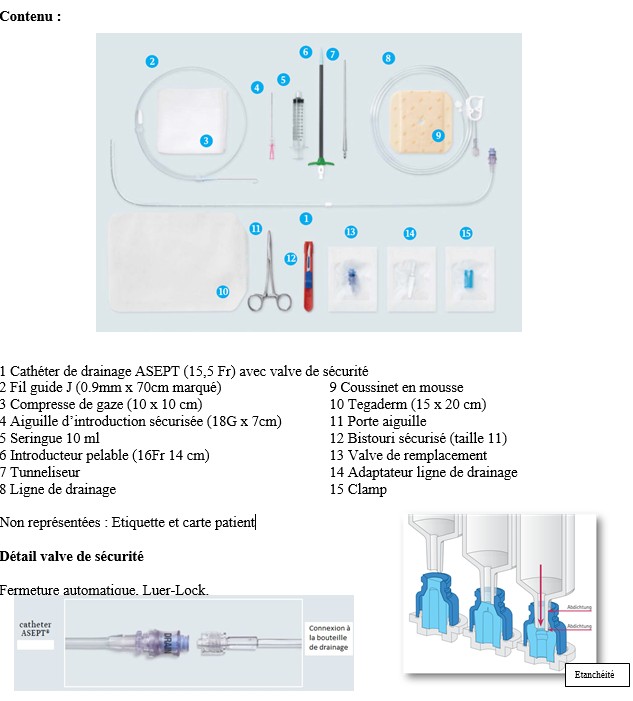
| Le système de drainage ASEPT est conçu pour le drainage pleural régulier et à long terme, dans le cadre des épanchements pleuraux , récurrents et symptomatiques.
Le système comprend tous les composants nécessaires à l'insertion tunnelisée du cathéter de drainage permanent ASEPT® selon la technique mini-invasive de Seldinger. La technique Seldinger minimise le risque de blessure des organes internes. L'intervention, qui se déroule sous anesthésie locale, peut être réalisée en hospitalisation ou en ambulatoire. Une manchette en polyester délimite la tunnelisation du cathéter, à la limite de la barrière sous-cutanée, elle favorise l’endothélialisation et minimise ainsi le risque de désinsertion du cathéter.
L’extrémité proximale du cathéter est dotée d’une valve qui empêche le fluide ou l’air de rentrer ou de sortir de la cavité jusqu’à l’activation de la valve. La valve de sécurité ASEPT® est comprise dans le kit, elle se ferme automatiquement, est facile à nettoyer et relie le cathéter au flacon de drainage de manière parfaitement hygiénique. Aucun embout ou fixation n'est nécessaire. La valve fonctionne en toute sécurité, même après de nombreuses connexions.
L’utilisation du système ASEPT présente un faible taux d'infection. D'une part, l'insertion tunnelisée du cathéter constitue une barrière efficace contre l'infection, d’autre part, les bouteilles de drainage qui sont sous pression négative empêchent les fluides contaminés de pénétrer dans l'espace d'épanchement.
|
| 2.7 |
Références catalogue : |
|
Référence :
P09080001
Descriptif :
Système de drainage pleural ASEPT®
Conditionnement :
UCD Unité de commande : 1 BOITE(S)
CDT Conditionnement : 1 BOITE(S)
QML Quantité mimimale de livraison : 1 UNITE(S)
Caractéristique(s) :
| |
|
| 2.8 |
Composition du dispositif et accessoires : |
| Principaux composants et matériaux :
|
CATHETER DE DRAINAGE
- SILICONE
COMPRESSE
- COTON
SERINGUE
- POLYPROPYLENE
PORTE AIGUILLE
- ACIER INOXYDABLE
BISTOURI
- ACIER INOXYDABLE
BISTOURI
- PLASTIQUE
|
| Substances actives : |
|
|
|
Pour les composants suceptibles d'entrer en contact avec le patient et/ou les produits administrés, précisions complémentaires
|
| Latex : |
Non |
| Phtalates : |
Non |
| Origine animale ou biologique : |
Non |
| Dispositifs et accessoires associés (consommables captifs notamment) : |
| -Les kits de drainage ASEPT® sont disponibles en deux tailles (600 ml référence P09080003 / 1000 ml référence P09080004) et contiennent les consommables nécessaires à leur utilisation.
- Valve de remplacement ASEPT® référence P09080005
- Ligne de drainage ASEPT® référence P09080006 |
| 2.9 |
Domaines et indications (selon nomenclature Euro-Pharmat) : |
| Domaines : |
|
|
| Indications (Informations complémentaires au paragraphe 6) : |
|
|
| 4. Conditions de conservation |
| |
Conditions normales de conservation et de stockage : |
| conserver dans un endroit sec et à l’abri de la lumière directe du soleil, dans une pièce à température modérée. |
| Précautions particulières : |
| - stérile et non pyrogène ; vérifier que le conditionnement fourni n’est ni ouvert, ni endommagé
- lire les instructions d’utilisation avant usage
- ne pas restériliser, usage unique
|
| Durée de validité du produit : |
| |
| Présence d'indicateurs de température (s'il y a lieu) : |
| |
| 5. Sécurité d'utilisation |
| 5.1 |
Sécurité technique : |
| |
| 5.2 |
Sécurité biologique (s'il y a lieu) : |
| |
| 6. Conseils d'utilisation |
| 6.1 |
Mode d'emploi : |
| |
| 6.2 |
Indications (destination marquage CE) : |
| Marquage CE 0124 |
| 6.3 |
Précautions d'emploi : |
| |
| 6.4 |
Contre indications (absolues et relatives) : |
| |
| 7. Informations complémentaires sur le produit |
| |
Informations complémentaires : |
| |
| 8. Documents annexés au dossier DM |
| |
|
| 9. Images (photos, étiquettes...) |
| |

|
Télécharger PDF Creator pour imprimer au format PDF
|